Organische Leuchtdiode – OLED
Bestimmte anorganische Halbleiter auf Siliziumbasis senden bei elektrischer Anregung sichtbares Licht aus. Diese Elektrolumineszenz ist bei den Lumineszenzdioden – LEDs beschrieben. Ein entsprechender Vorgang verursacht eine Lichtemission bei besonderen organischen Molekülen. Die technische Umsetzung begann 1987 durch eine Forschergruppe der Firma Kodak. In Anlehnung an die LEDs werden sie OLEDs organic light emittig diodes genannt.
Organische Fluoreszenzfarbstoffe
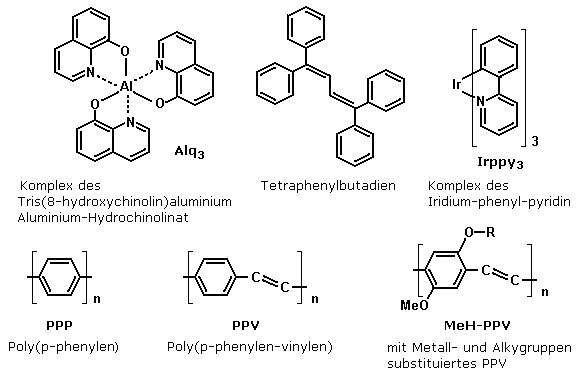
Der Emitterfarbstoff der OLEDs besteht aus kleineren organischen Verbindungen wie in der oberen Bildreihe oder aus langkettigen Polymeren, wie in der unteren Bildreihe gezeigt. Letztere werden auch PLEDs genannt. Zur Darstellung eines Farbbilds stehen alle Lichtfarben zur Verfügung. Die Lichtausbeute und die Lebensdauer der Luminophore ist aber noch recht unterschiedlich. Mit Iridium- und anderen Edelmetallkomplexen erschloss die BASF in den Jahren 2003/2004 den blauen Farbbereich. Das IrPPY3 emittiert grünes Licht. Die Displays mit den organischen Molekülen müssen gegen Feuchtigkeit und Sauerstoff versiegelt werden. Die Herstellung erfolgt unter den gleichen Reinheitsbedingungen wie bei anorganischen Halbleitern.
Der interne Aufbau und die Funktion der OLEDs
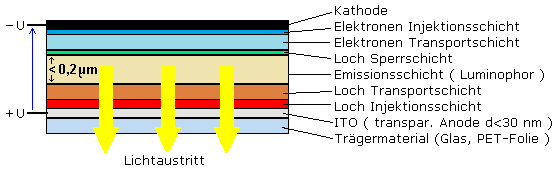
Der schematische Aufbau einer OLED ist recht einfach. Bei der Einschicht-OLED befindet sich die Licht aussendende organische Schicht zwischen zwei Elektroden. Die durchsichtige Anode ist und auf einen Glas- oder flexiblen Kunststoffträger aufgebracht. Das transparente Anodenmaterial ist Indium-Zinn-Oxid (ITO = indium-tin-oxid). Für die Kathode, die schon bei geringer Energiezufuhr Elektronen abgeben sollte, kommen Metalle wie Magnesium, Kalzium, Barium oder Aluminium infrage, die im Vakuum aufgedampft werden.
Praktisch nutzbar wurden OLEDs erst durch eine Mehrschichtenfolge, die in der Skizze unten dargestellt ist. Auf einen Träger aus Glas- oder Kunststofffolie wird die ITO-Anode aufgedampft. Es folgt eine Lochinjektionsschicht zum Transport der Defektelektronen, die positiven Ladungen oder Elektronenlöcher. Sie glättet die Anodenoberfläche und erhöht damit die Effizienz. Den gleichmäßigen Transport der positiven Ladungen in die Emissionsschicht besorgt eine Lochtransportschicht aus organischen Molekülen. In der Emissionsschicht rekombinieren die Ladungen. Dabei entstehen angeregte Molekülzustände, die durch Abgabe von Photonen in den energetischen Grundzustand wechseln. Das Licht gelangt durch die transparente ITO Anode nach außen. In Richtung Kathode verhindert eine Lochsperrschicht das Eindiffundieren positiver Ladungen in die organische Transsportschicht für Elektronen und verlängert somit die Lebensdauer der OLED. Die letzte organische Schicht ist über Lithiumfluorid, das als ohmscher Kontakt wirkt, mit der Metallkathode verbunden.
Fabrikationsverfahren für OLEDs
Die Luminophore können eigenständig oder in einer Matrix verteilt aufgebracht werden. OLEDs aus niedermolekularen Emitterfarbstoffen in einer polymeren Matrix werden als MDP, molekular dotierte Polymere bezeichnet. Hochmolekulare Emitterfarbstoffe in einer Polymermatrix werden Blends genannt. Das Matrixmaterial ist vielfach Polystyrol oder Polymethacrylat, ein Plexiglasderivat.
Die niedermolekularen Luminophore lassen sich als Pulver herstellen und im Vakuum durch Sublimation aufdampfen. Durch Anwenden eines Maskenverfahrens lassen sich verschieden farbige Pixelfolgen aufbringen. Hochpolymere Luminophore und Matrixmischungen werden aus einer flüssigen Phase durch das Spincoating Verfahren aufgebracht. Eine Polymerlösung tropft zentral auf den schnell rotierenden Träger und wird gleichmäßig darauf verteilt. Abschließend wird das Lösungsmittel verdampft.
Das Funktionsprinzip der OLEDs
Zwischen der Strom leitenden ITO-Anode und einer Metallkathode befindet sich eine organische Emitterschicht mit weitgehend isolierenden Eigenschaften. Der Schichtenaufbau entspricht dem eines Kondensators. Ein außen angelegtes elektrisches Feld bringt die Elektronenverteilung der Emittermoleküle in einen angeregten Zustand. Der Energieausgleich erfolgt durch Fluoreszenzstrahlung, einer Photonenemission im sichtbaren Bereich.
Die Elektronenverteilung in den Molekülen unterliegt physikalischen Gesetzen, wobei die energetisch tiefer liegenden Orbitale zuerst besetzt und aufgefüllt werden. In Molekülverbindungen spalten sich die einzelnen Atomorbitale in mehrere nahe beieinanderliegende Molekülorbitale, den Orbitalbändern, auf. Das äußere mit Elektronen besetzte Band ist das Valenzband. Es wird auch als HOMO, highest occupied molecular orbital, das höchste besetzte Molekülorbital bezeichnet. Das energetisch höher liegende und bei Isolatoren unbesetzte Orbitalband ist das Leitungsband. Man bezeichnet es auch als LUMO, lowest unoccupied molecular orbital, das niedrigste unbesetzte Molekülorbital.
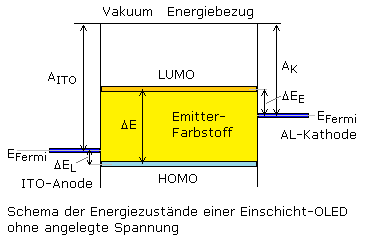
EFermi: Fermi-Energie von Anode und Kathode.
AK: Elektronenaustrittsarbeit der Kathode.
AITO: Elektronenaustrittsarbeit der Anode 4,7 eV.
ΔEE: Energiebarriere mit 0,3 ... 0,4 eV für Elektronen bei Injektion in den Emitter.
ΔEL: Energiebarriere mit 0,3 ... 0,4 eV für Löcher bei Injektion in den Emitter.
ΔE: Bandlücke des Emitters mit 3,2 ... 1,6 eV bestimmt die Wellenlänge des emittierten Lichts.
Zwischen HOMO und LUMO besteht eine Energiedifferenz. Liegt Spannung an den Elektroden an, und ist die Anode positiv gegenüber der Kathode, verschieben sich die Energieniveaus. Elektronen werden von der Kathode ins LUMO injiziert. Gleichzeitig zieht die Anode Elektronen aus dem HOMO ab und schließt den äußeren Stromkreis. Der Anodenvorgang entspricht der Injektion von Defektelektronen, den Elektronenlöchern in das HOMO. Elektronen und Löcher wandern in entgegengesetzte Richtungen. Die meisten werden an den Elektroden entladen. Einige rekombinieren zu Singulett-Excitonen. Diese besonderen Elektronen-Lochpaare zerstrahlen unter Photonenabgabe.
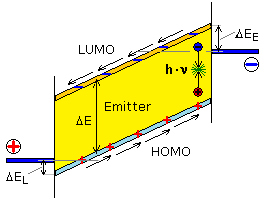
Das Energieschema zeigt zwischen den Elektroden und dem Emitter Energiebarrieren, die bei der Ladungsträgerinjektion überwunden werden müssen. Je besser die Elektroden an die Energieniveaus des Emitters angepasst sind, desto geringer ist die Betriebsspannung für die Lichtemission. Es werden Kathoden mit geringer Austrittsarbeit für die Elektronenabgabe benötigt. Diese Eigenschaft weisen unedle Metalle wie Magnesium, Kalzium, Barium, Aluminium auf. Die Anode muss eine hohe Austrittsarbeit für Elektronen, dafür aber eine große Elektronenaffinität aufweisen. Diese Bedingung wird vom transparenten ITO-Material sehr gut erfüllt.
Ein Elektronen- und Lochtransport im gleichen Material kann mittels Redoxprozesse beschrieben werden. Leicht reduzierbare Substanzen ergeben gute Elektronenleiter. Die organischen Emitterhalbleiter sind leicht oxidierbare Stoffe und daher gute Lochleiter. Wegen des schnelleren Lochtransports erfolgt die Rekombination und Lichtaussendung bevorzugt an der Grenzfläche zur Kathode. Dieser Bereich hat herstellungsbedingt nicht die erforderliche Reinheit und der Energieausgleich der Excitonen liefert daher eine zu geringe Photonenausbeute.
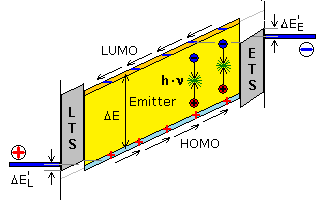
OLEDs mit hohem Wirkungsgrad bei gleichzeitig verlängerter Lebensdauer werden im Mehrschichtverfahren hergestellt. Zwischen Kathode und Emitter wird eine Elektronentransportschicht (ETS) und zwischen Anode und Emitter eine Lochtransportschicht (LTS) angeordnet. Beides sind nicht kristalline organische Substanzen, die zu dünnen Filmen aufsublimiert werden. Sie erleichtern zudem die Ladungsträgerinjektion in den Emitter und verlagern die Rekombinationszone in die Mitte der Luminophore.
Die elektrische Steuerung der OLEDs
OLED Displays lassen sich mit passiver und aktiver Matrix steuern. Bei der einfacheren passiven Matrix liegt zwischen jedem Kreuzungspunkt von Anode und Kathode ein Bildpunkt. Die ITO-Anode kann zum Teil vollflächig ausgeführt sein. Wie bei den ersten passiven LCD-Displays werden auch hier die Bildpunkte durch eine getrennte Zeilen- und Spaltenansteuerung gesteuert. Ohmsche Verluste bei der Stromleitung im Display begrenzen bei einer Passivansteuerung die Anzeigefläche auf diagonal 5 cm.
Große und für eine detaillierte Bildwiedergabe geeignete Displays werden mit aktiver Matrix gesteuert. Jeder Bildpunkt erhält seinen eigenen Dünnfilmtransistor. Die Steuertechniken sind von den TFT-LCD-Flachbildschirmen her erprobt. Die bestehenden Fertigungsprozesse konnten für OLED-Displays angepasst werden.
Rekombination der Ladungsträgerpaare in einer OLED
In den organischen Emitterfarbstoffen liegen Elektronenpaarbindungen vor. Im Elektronenpaar müssen sich die Einzelelektronen durch einen entgegengesetzten Eigendrehimpuls, dem Elektronenspin unterscheiden. In allen Molekülen sind die Energiezustände der Elektronenorbitale aufgespalten. Ihre Besetzung durch die Elektronen erfolgt nach genau definierten Regeln.
Werden die Moleküle energetisch angeregt, so gelangen einzelne Elektronen aus ihrem Grundzustand in das LUMO, das Leitfähigkeitsband. Je nach Spinlagen ergeben sich angeregte Singulett- oder Triplett-Zustände. Der Singulett-Zustand ist energiereicher und für die Fluoreszenzstrahlung verantwortlich. Der Grundzustand vieler organischer Moleküle ist ein Singulett. Da quantenphysikalisch nur gleichartige Übergänge erlaubt sind, werden fast alle niedermolekularen Emitterfarbstoffe als Singulett-Emitter genutzt. Dabei lassen sich nur 25 % der zugeführten elektrischen Energie in Photonenstrahlung umwandeln. Die verbleibenden 75 % ergeben Triplett-Zustände. Rekombinieren diese Elektronen-Lochpaare, so entsteht langwelligere und damit unsichtbare Wärmestrahlung. Triplett-Singulett-Übergänge rechnen zu den verbotenen Übergängen und erzeugen Phosphoreszenzstrahlung.
Seit 1998 werden in der OLED-Technologie auch Triplett-Emitter eingesetzt. Die andauernde Forschung sucht nach geeigneten metallorganischen Komplexverbindungen, deren Lichtemission aus einem schnellen Triplett-Singulett-Übergang erfolgt. Die Photonenausbeute kann dann auf das Dreifache ansteigen. Ein weiterer Forschungszweig befasst sich mit dem Intersystem-Crossing. Der energetisch höhere Singulett-Zustand wechselt unter Spinumkehr in einen angeregten tieferen Triplett-Zustand. In Gegenwart bestimmter Schwermetalle wie Iridium oder Platin rekombinieren die Excitonen von dort in weniger als 100 ns sehr schnell durch Phosphoreszenzstrahlung im sichtbaren Bereich.
Vor- und Nachteile der OLEDs
Im Vergleich zu den LEDs auf Siliziumtechnik und den LCD-Displays bieten OLEDs folgende Vorteile:
- Vorteile
- Mit OLEDs lassen sich gleichmäßig hell leuchtende, großflächige Einzeldioden herstellen.
- OLEDs können in beliebigen Strukturen und Mustern gefertigt werden.
- OLEDs sind sehr dünn und auch auf flexiblen Trägerfolien produzierbar.
- Die Betriebsspannung liegt um 5 V. Der Strombedarf ist geringer als bei LEDs
- OLEDs sind videotauglich und haben viel kürzere Schaltzeiten als TFT-LCDs.
- OLEDs haben verglichen mit TFT-LCDs den besseren Kontrast ohne Einschränkung des Blickwinkels.
- OLED-Displays leuchten selber und benötigen keine Hintergrundbeleuchtung wie LCDs.
- OLEDs haben einen großen Temperaturbereich und arbeiten auch bei Minusgraden einwandfrei.
- Bei RGB-Video- und Farbbilddisplays entfallen Licht absorbierende Farb- und Polarisationsfilter.
- Die Herstellungskosten sind niedriger da die aufwendigen Dotierungsprozesse der Si-Dioden entfallen.
Noch gibt es einige Nachteile bei OLEDs, die einer sofortigen Markteroberung entgegen stehen:
- Nachteile
- Die Emitterfarbstoffe sind empfindlich gegen Oxidation und Feuchtigkeit.
- Die mittlere Lebensdauer der RGB-Farben ist noch zu unterschiedlich.
- Die Leuchtintensität nimmt zu kürzeren Wellenlängen schneller ab, es entstehen Fehler durch Farbverschiebung.
- Eine große Leuchtstärke beschleunigt den Intensitätsverlust und verkürzt die Lebensdauer.